Alors qu’une des conceptions les plus communes de la pollinisation est le cas des abeilles et du miel qu’elles produisent, bien d’autres animaux – oiseaux, rongeurs, lézards – interagissent avec les fleurs et les fécondent. La recherche dans le domaine de la pollinisation tente de comprendre comment les plantes attirent ces bêtes nectarivores afin de clore leur cycle de reproduction. Dans un monde marqué par les changements climatiques et les pressions humaines, ces informations permettront de déterminer quel sera leur devenir. C’est dans cette optique que des chercheurs de l’Institut de recherche de biologie végétale de l’Université de Montréal (IRBV) se penchent sur ces interactions entre fleurs et visiteurs afin de mieux connaître l’évolution des plantes à fleurs.
Peu après la tombée de la nuit, une chauve-souris haïtienne virevolte autour d’une gesnériacée antillaise (voir la figure 1). C’est dans les fleurs de cette plante buissonneuse que le mammifère volant trouvera nourriture et énergie, sous la forme d’un nectar translucide, épais et sucré. Bien que la vue du chiroptère ne soit pas bonne, le parfum sucré diffusé par ces étranges fleurs orange spécialement pour l’attirer permet à l’animal de facilement suivre le chemin jusqu’à la ressource tant désirée. Sur les hauts plateaux haïtiens comme dans les prairies québécoises, les plantes attirent les animaux… et leur offrent du nectar en échange. Près de 260 000 plantes à fleurs terrestres ont ainsi développé une stratégie d’attraction pour presque 300 000 espèces d’insectes, d’oiseaux et de mammifères nectarivores[1]. En revanche, derrière chacune de ces interactions entre plante et pollinisateur se cachent des histoires de séduction, de manipulation et de déception insoupçonnées.
Rhytidophyllum bicolor, observée dans le parc national Macaya en Haïti
Source : Julie Faure
L’adaptation des plantes
Bien qu’amorcée par Charles Darwin en 1877 avec son étude sur les orchidées[2], la recherche dans le domaine de la pollinisation est toujours fortement active, puisque les relations complexes entre pollinisateur et plante n’ont pas encore dévoilé tous leurs secrets. À Montréal, les études du laboratoire du professeur Simon Joly, botaniste chercheur à l’IRBV, se focalisent sur les gesnériacées antillaises, famille dont l’espèce sœur la plus connue est la violette africaineSaintpaulia ionantha. Pour l’étude de la pollinisation, ces plantes forment un sujet de recherche idéal, car les fleurs de cette famille peuvent être pollinisées par des colibris, des chauves-souris, des abeilles, des papillons de nuit ou par une combinaison de plusieurs de ces animaux[3]. En s’intéressant à 18 espèces de gesnériacées antillaises visitées par les colibris, une nouvelle étude de l’équipe du laboratoire qui n’a pas encore été publiée a pu démontrer que ces fleurs ont une forme très semblable au bec des visiteurs récurrents. Cette famille de plantes s’est donc fortement adaptée à des espèces particulières d’animaux, qui deviennent ainsi les principaux pollinisateurs de la fleur. Or, ce ne sont pas toutes les gesnériacées antillaises qui l’ont fait. Une autre étude récente du même laboratoire, finalisée mais non publiée, montre que la stratégie de pollinisation généraliste, c’est-à-dire quand les fleurs sont visitées par plusieurs animaux différents, est un atout face aux perturbations naturelles, qui peuvent avoir des répercussions sur l’abondance des espèces pollinisatrices. Par exemple, un an après le passage d’un ouragan en Haïti, les fleurs de l’espèce Rhytidophyllum bicolor étaient toujours visitées par les chauves-souris et les abeilles, bien que les colibris, pollinisateurs importants, ne fussent plus présents. Ainsi, une plante trop adaptée à un animal particulier pourrait voir son cycle reproductif stoppé si l’animal ne se trouve plus dans le milieu.
Les traits floraux
Lorsqu’un animal particulier pollinise les fleurs d’une espèce végétale, celle-ci développe des traits floraux caractéristiques qui l’attireront plus efficacement. Une fleur de pétunia, par exemple, est pollinisée principalement par les papillons et les colibris et présente ainsi une forme de trompette, mieux adaptée au bec ou à la trompe de ses visiteurs. Ce phénomène s’appelle le « syndrome de pollinisation* » ou la « stratégie de pollinisation »[4]. Ce syndrome peut être exprimé sous la forme d’une couleur ou d’une forme florale particulières, d’un parfum envoûtant, ou encore d’un nectar plus ou moins sucré et produit à différentes heures de la journée. Par exemple, une fleur aura plus de probabilité d’être visitée par un colibri si elle est rouge, puisqu’elle contrastera ainsi avec la végétation environnante. Une chauve-souris, quant à elle, préférera les fleurs s’ouvrant la nuit et dont le parfum est détectable de loin. Celles-ci seront souvent pâles, blanches ou vertes, car les couleurs vives ne sont plus sous pression de sélection, n’étant pas plus visibles la nuit. Pour les abeilles, les fleurs qui auront le plus de succès seront majoritairement violettes, puisqu’elles reflètent les rayons solaires ultraviolets qui sont détectés par la vision des insectes, et présenteront souvent un pétale du bas assez large fournissant une « piste d’atterrissage », comme c’est le cas de la violette du Canada, Viola canadensis. Les traits floraux exprimés par une espèce permettent de supposer quels animaux la visiteront.
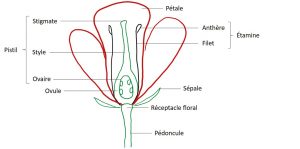
L’intérêt se porte alors sur l’avantage de la plante à attirer des animaux particuliers dans ses fleurs. En effet, pour que le cycle de reproduction soit complet, les grains de pollen présents sur les étamines* d’une fleur doivent être déposés sur le pistil* pour pouvoir atteindre les ovules et pour que des graines soient produites après la fécondation (voir la figure 2). Pour assurer la continuité de son cycle de reproduction, une fleur peut recourir à diverses stratégies : elle peut s’autopolliniser*, disséminer son pollen par le vent ou l’eau ou bien utiliser d’autres êtres vivants (par exemple, des animaux) pour faire passer son pollen d’une plante à une autre.
Coupe d’une fleur
Source : Julie Faure
Une relation mutualiste
Si l’autopollinisation* est commune chez plusieurs plantes et que la dissémination par le vent est très utilisée par les graminées cultivées (blé, orge, autres céréales), c’est toutefois la stratégie d’utilisation des animaux qui se retrouve chez les gesnériacées antillaises, mais aussi chez 87 % des plantes à fleurs à travers le globe[5] et chez 70 % des plantes cultivées[6]. Le jeu de séduction entre les plantes et les pollinisateurs s’est grandement diversifié au moment de l’apparition des plantes à fleurs, les angiospermes*, il y a environ 135 millions d’années[7]. Cette tactique d’attraction a visiblement porté ses fruits, puisque les animaux qui sont aujourd’hui attirés par ces beaux attraits sont nombreux (abeilles, bourdons, papillons, mouches, souris, escargots, lémurs, etc.).
Un des exemples les plus connus de zoogamie* et aussi celui qui permet le mieux de comprendre l’intérêt pour un animal à visiter une fleur est sans aucun doute le cas des abeilles domestiques. En plus de présenter des caractères floraux particulièrement attractifs pour l’animal pollinisateur, la fleur produit un nectar riche en sucre qui fera office de récompense pour le visiteur. Dans l’exemple des abeilles domestiques, en aspirant le nectar servant à produire le miel nécessaire au développement de leur colonie, celles-ci récupèrent au passage de nombreux grains de pollen, qu’elles déposeront sur la prochaine fleur butinée. De cette façon, chaque protagoniste trouve son compte – le pollinisateur se nourrit et participe en échange activement à la pollinisation – dans ce qui s’appelle une relation mutualiste*, puisqu’elle bénéficie à tous.
La vraie manipulation
Si la production de nectar a pour but d’attirer et de récompenser le pollinisateur, l’animal qui vient s’en nourrir ne dépose le pollen dans d’autres fleurs de la même espèce que de façon accidentelle. En effet, pour accéder au précieux nectar, le pollinisateur doit se frotter aux étamines, ce qui permet au pollen qui s’y trouve au départ de se coller à ses poils ou à ses plumes. En allant par la suite se nourrir sur une autre fleur de la même espèce, le pollinisateur se frottera également au pistil de la nouvelle fleur, déposant ainsi le pollen clandestin sur celui-ci et achevant le cycle reproducteur. Bien que bénéfique aux deux parties, cette interaction peut être perçue comme une « manipulation » de la part de la plante. Ce terme est d’autant plus vrai dans le cas de plusieurs espèces de plantes qui ont évolué pour ne plus produire de nectar, mais qui attirent encore les pollinisateurs grâce à leurs autres traits floraux, comme leur couleur ou leur forme.
Un exemple est celui des orchidées du genre Ophrys (voir la figure 3). Les fleurs de ces espèces ressemblent souvent à s’y méprendre à une femelle insecte (abeille, bourdon, etc.) et libèrent de plus une odeur semblable à celle-ci. Le mâle dupé viendra en contact avec les parties reproductives de la plante, croyant s’accoupler avec sa bien-aimée. Une fois le subterfuge révélé, le visiteur repartira sans récompense, mais en emportant du pollen à son insu[8].
Plus près de Montréal, le sabot de la vierge (voir la figure 4), Cypripedium acaule, qui se rencontre dans les forêts et les milieux humides du Québec, utilise un autre type de supercherie. Attiré par l’odeur sucrée sécrétée par la fleur zygomorphe* ainsi que par ses belles couleurs jaune et rose, le bourdon entre par un orifice situé dans le labelle*.Cependant, une fois à l’intérieur, en plus de constater l’absence de nectar, le pollinisateur se rend vite compte qu’il ne peut plus sortir par le même orifice, à cause des marges repliées de celui-ci. Une seule voie de sortie s’offre à lui : il doit ramper et grimper jusqu’à un autre accès étroit plus haut dans la fleur. Ce passage étroit oblige l’insecte à se frotter contre le pistil et les étamines, qui déposent ainsi du pollen sur son corps. Lors de sa prochaine visite d’une fleur de la même espèce, le visiteur permettra la pollinisation, sans pour autant trouver le nectar recherché[9].

Figure 3 : Fleur d’ophrys bourdon, Ophrys fuciflora ; figure 4 : fleur de sabot de la vierge, Cypripedium acaule
Source : Figure 3 : Cakie. (2012). Un bourdon très attirant. Des fleurs à notre porte. http://desfleursanotreporte.over-blog.com/article-un-bourdon-tres-attirant-106254482.html ; figure 4 : Cypripedium acaule – Sabot de la vierge. (s. d.). https://www.plantes.ca/fleurs/famille/cypripedium-acaule.html
Une compréhension nécessaire
Chez les gesnériacées antillaises, la séduction se fait par des traits floraux spécifiques adaptés à la morphologie des pollinisateurs et par la couleur de la corolle : les fleurs rouges et tubulaires attirent les colibris, alors que celles de couleur verte en forme de cloche attirent les chauves-souris. En étudiant les traits floraux, les recherches visent à mieux comprendre l’écologie de ces plantes et leur histoire évolutive. En effet, la notion de stratégie de pollinisation permet d’émettre des hypothèses sur le type de pollinisateurs qu’attire une fleur, même si ceux-ci n’ont pas été observés. Les données de traits floraux d’une espèce fossile permettent de supposer quel était l’animal la visitant ainsi que de retracer l’évolution des adaptations florales d’une plante et ses changements de syndrome de pollinisation tout au long de son évolution et de sa colonisation de nouveaux habitats. De la même façon, l’analyse des stratégies de reproduction permet de prévoir l’évolution future d’une plante grâce à sa stratégie de pollinisation, comme montré dans l’étude non encore publiée de l’IRBV d’une espèce généraliste en Haïti face à des perturbations naturelles.
À une époque où la perte de pollinisateurs et les changements climatiques pourraient avoir des effets dévastateurs sur les plantes[10], l’étude des traits floraux et de l’évolution des plantes peut permettre de mieux protéger celles-ci. Savoir comment une plante a évolué au cours du temps et connaître sa capacité à s’acclimater ou à tolérer de nouveaux environnements et pollinisateurs permet de prédire si elle sera capable de s’adapter à des changements radicaux tels que les changements climatiques, la perte de pollinisateurs en raison de l’utilisation de pesticides ou la perte d’habitat par la propagation de l’urbanisation, qui peuvent changer les communautés animales présentes dans les écosystèmes[11]. Dans de tels cas, une plante qui ne peut s’adapter assez rapidement parce que ses traits floraux ou sa forme visent trop l’attraction de visiteurs particuliers a de grandes chances de disparaître. Puisque 70 % des plantes cultivées dans le monde reposent sur la pollinisation des animaux, la conservation de ces plantes et de leurs pollinisateurs est plus que jamais un sujet d’actualité.
Lexique :
Angiosperme : division de plantes vasculaires du groupe des spermatophytes (plantes à graines), qui comprend toutes les plantes portant des fleurs, puis des fruits.
Autopollinisation : déplacement d’un grain de pollen d’une fleur vers le stigmate (extrémité supérieure du pistil) de la même fleur ou d’une fleur de la même plante, qui aboutit à une autofécondation si l’espèce est autocompatible.
Étamine : unité de l’appareil reproducteur mâle (androcée) chez les plantes à fleurs. Elle se compose d’un filet et d’une anthère au sommet, qui porte les loges produisant et contenant le pollen.
Labelle : troisième pétale modifié de la fleur des orchidées. Il est de forme, de taille et de couleurs très variées selon les espèces. Sa fonction est essentiellement d’attirer l’insecte pollinisateur vers le cœur de la fleur et il permet souvent à l’insecte de se poser. Chez Cypripedium, il est particulièrement gros et gonflé.
Pistil : appareil reproducteur femelle chez les plantes à fleurs, aussi appelé « gynécée ». Il est formé d’un ou de plusieurs carpelles contenant les ovules.
Relation mutualiste : interaction entre différentes espèces dans laquelle chaque organisme impliqué tire des avantages, gains ou profits.
Syndrome de pollinisation : ensemble de traits floraux (forme, couleur, odeur, type de nectar, etc.) résultant de l’adaptation à un vecteur de pollinisation biotique (pollinisateurs : oiseaux, insectes, etc.) ou abiotique (vent, eau).
Zygormorphe : se dit d’une fleur présentant une symétrie bilatérale, c’est-à-dire sur un seul plan vertical. Les orchidées ou les violettes, par exemple, présentent des fleurs zygomorphes.
Zoogamie : forme de pollinisation réalisée par les animaux.
Références
[1] González-Varo, J. P., Biesmeijer, J. C., Bommarco, R., Potts, S. G., Schweiger, O., Smith, H. G., Steffan-Dewenter, I., Szentgyörgyi, H., Woyciechowski, M. et Vilà, M. (2013). Combined effects of global change pressures on animal-mediated pollination. Trends in Ecology & Evolution, 28(9), 524-530. https://doi.org/10.1016/j.tree.2013.05.008
[2] Darwin, C. (1877). The various contrivances by which orchids are fertilised by insects. John Murray.
[3] Skog, L. E. (1976). A study of the tribe Gesneriaceae, with a revision of Gesneria (Gesneriaceae-Gesnerioideae).Smithsonian Contributions to Botany.
[4] Faegri, K. et Van Der Pijl, L. (2013). Principles of pollination ecology. Elsevier.
Fenster, C. B., Armbruster, W. S., Wilson, P., Dudash, M. R. et Thomson, J. D. (2004). Pollination syndromes and floral specialization. Annual Review of Ecology, Evolution, and Systematics, 35, 375-403. https://doi.org/10.1146/annurev.ecolsys.34.011802.132347
[5] Ollerton, J., Winfree, R. et Tarrant, S. (2011). How many flowering plants are pollinated by animals?. Oikos, 120(3), 321-326. https://doi.org/10.1111/j.1600-0706.2010.18644.x
[6] Klein, A. M., Vaissiere, B. E., Cane, J. H., Steffan-Dewenter, I., Cunningham, S. A., Kremen, C. et Tscharntke, T. (2007). Importance of pollinators in changing landscapes for world crops. Proceedings of the royal society B: Biological sciences, 274(1608), 303-313. https://doi.org/10.1098/rspb.2006.3721
[7] Magallón, S., Gómez‐Acevedo, S., Sánchez‐Reyes, L. L. et Hernández‐Hernández, T. (2015). A metacalibrated time‐tree documents the early rise of flowering plant phylogenetic diversity. New Phytologist, 207(2), 437-453. https://doi.org/10.1111/nph.13264
[8] Borg-Karlson, A. K. (1990). Chemical and ethological studies of pollination in the genus Ophrys (orchidaceae). Phytochemistry, 29(5), 1359-1387. https://doi.org/10.1016/0031-9422(90)80086-V
[9] Davis, R. W. (1986). The pollination biology of Cypripedium acaule (orchidaceae). Rhodora, 88(856), 445-450. https://www.jstor.org/stable/23314206
[10] Nolan, C., Overpeck, J. T., Allen, J. R., Anderson, P. M., Betancourt, J. L., Binney, H. A., … Djamali, M. (2018). Past and future global transformation of terrestrial ecosystems under climate change. Science, 361(6405), 920-923.
González-Varo et al., op. cit.
[11] Wenzel, A., Grass, I., Belavadi, V. V. et Tscharntke, T. (2020). How urbanization is driving pollinator diversity and pollination–A systematic review. Biological Conservation, 241, 108321. https://doi.org/10.1016/j.biocon.2019.108321