Contrairement à ce que bien des gens croient, l’Arctique canadien ne peut plus être considéré comme un environnement vierge et isolé de toutes sources de pollution provenant du monde industriel. Les études récentes démontrent en effet la présence croissante et très inquiétante de nombreux contaminants chimiques dans les écosystèmes de l’Arctique1. Le mercure est l’un des contaminants les plus dangereux et prioritaires, avec une toxicité inhérente élevée, posant un risque important pour la santé écosystémique et humaine.
Vous êtes-vous déjà imaginé au milieu de l’Arctique canadien, entouré de vastes champs de neige éternelle? Vous croyez peut-être que l’Arctique est une vaste réserve naturelle, un environnement polaire isolé, loin de toutes les sources de pollution, qui s’amplifient dans de basses latitudes depuis l’ère industrielle. Il est vrai que l’Arctique demeure un endroit relativement propre par rapport aux autres régions du monde. Cependant, les études récentes démontrent la présence croissante et très inquiétante de nombreux contaminants chimiques dans les écosystèmes terrestres et aquatiques de l’Arctique1,2. Ces contaminants néfastes regroupent les polluants organiques persistants (ou POP) qui se dégradent très lentement dans l’environnement, tels que le DDT* et les BCP*, ainsi que les métaux lourds, tels que le mercure (Hg). Certains scientifiques affirment même que l’Arctique est devenu un puits de contaminants toxiques arrivant des quatre coins du monde[1],[2].
En octobre 2013, un nouvel accord international désigné La convention de Minamata sur le mercure a été signé par 92 différents pays, affirmant que le mercure est l’un des contaminants les plus prioritaires de nos jours, à une échelle mondiale. Les écosystèmes arctiques sont particulièrement vulnérables à une contamination au mercure, qui s’accumule à de hautes concentrations dans les réseaux alimentaires arctiques3. Depuis l’ère préindustrielle, les concentrations de mercure ont augmenté de 2 à 3 fois dans les sédiments des lacs arctiques et de 10 fois dans l’organisme des grands prédateurs arctiques tels que les bélugas, phoques, ours et oiseaux de proie1. Les écosystèmes arctiques sont aussi parmi les plus vulnérables aux impacts des changements climatiques*, qui risquent d’influencer le cycle de mercure dans l’environnement de manière significative3,4.
Quelles sont les conséquences d’une contamination au mercure? Le mercure est une neurotoxine dangereuse pour les systèmes nerveux et endocrinien chez les vertébrés, qui peut passer des poissons aux humains. Une exposition élevée au mercure induit une perte de coordination, une incapacité à se nourrir, une réduction de la réactivité et une sensibilité accrue à la maladie1,7. Chez les peuples autochtones de l’Arctique, les nouveau-nés de mères ayant subi une exposition élevée au mercure ont plus de risques de manifester des troubles de développement neurologiques et comportementaux1.
Provenance du mercure de l’Arctique
Les études récentes soulignent le fait étonnant que les principales sources de la contamination de l’Arctique sont les pays situés en zones tempérées1. Le mercure se rend en Arctique principalement, et très rapidement, par voie atmosphérique. Il y est aussi transporté, plus lentement, par les courants océaniques, les rivières, la dérive des glaces de mer et plusieurs espèces migratrices1,4. La plus grande partie d’émissions anthropiques de mercure, environ 50 % du total mondial, viennent des émissions atmosphériques de l’Asie, notamment de la Chine. La principale source d’émissions est la combustion de charbon dans les centrales thermiques en Asie, mais aussi en Europe et en Amérique du Nord3. En effet, comme le mercure se trouve naturellement un peu partout dans le sol, y compris dans les gisements de charbon, la combustion de charbon libère du mercure dans l’atmosphère.
Dans un processus qu’on appelle la distillation globale, les contaminants semi-volatils* sont vaporisés dans l’atmosphère en zone tempérée pour être ensuite transportés en Arctique par les courants atmosphériques dominants5. Cette distillation se produit de la même manière que la distillation employée dans la production d’alcool ou dans la purification de l’eau de mer pour obtenir de l’eau douce, mais à une échelle beaucoup plus grande!
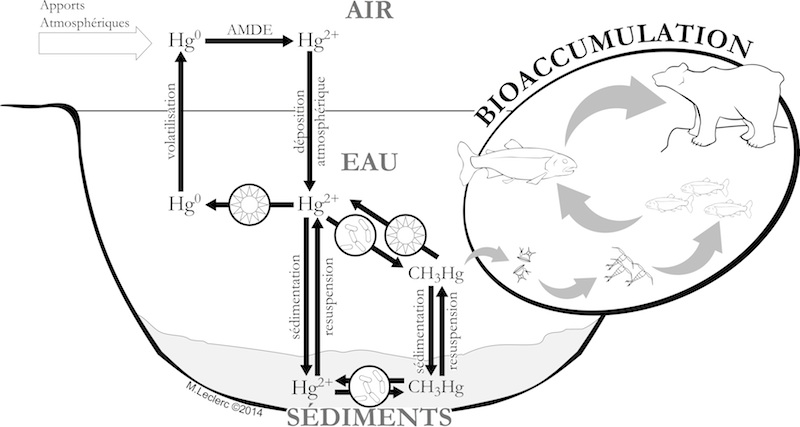
Imaginez un atome de mercure inorganique (ou Hg(II)) enfoui dans un dépôt géologique de charbon au nord de la Chine. Dans une mine de charbon à ciel ouvert, les ouvriers chinois exploitent ce gisement et cet atome de mercure est extrait, puis transporté par camion jusqu’à une centrale thermique à Beijing. Quand le charbon est brûlé à haute température, le Hg(II) est émis par les cheminées sous sa forme volatile, le Hg métallique ou Hg(0)5,6. Ce petit atome de Hg(0) demeure dans l’atmosphère pendant plus d’un an, voyageant sur une très grande distance et porté par les vents dominants de la Chine vers le nord du Canada. Au-dessus de l’île de Baffin dans l’Arctique, l’atome de Hg(0) est soumis à une oxydation atmosphérique en raison du lever de soleil polaire au printemps. Il se dépose ensuite sur la surface d’un lac sous sa forme oxydée, le Hg(II)5,6. L’atome de Hg(II) se lie rapidement à de la matière en suspension dans l’eau et tombe dans le fond du lac, proche des sédiments. Par la suite, le Hg inorganique (Hg(II)) est transformé en Hg organique ou en méthylmercure (la forme la plus toxique de ce contaminant) grâce à l’activité des microorganismes (voir fig. 1)1,6.
Cheminement du méthylmercure dans l’Arctique
Le mercure dans l’Arctique est devenu une préoccupation prioritaire à la suite de la découverte que de nombreux prédateurs au sommet des réseaux trophiques* y sont contaminés, comme le béluga, l’ours polaire, le phoque annelé et l’humain1.
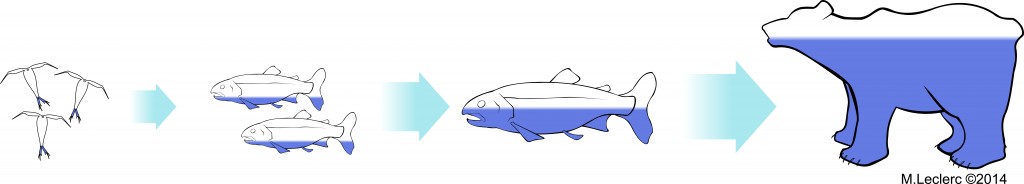
Comment ce contaminant s’accumule-t-il dans les organismes de l’Arctique? Comme le taux d’élimination de Hg est très lent par rapport à son taux d’assimilation, le Hg s’accumule au sein des organismes aquatiques par le processus de bioaccumulation*, c’est-à-dire l’assimilation des contaminants provenant des sols, de l’eau, de l’air et de la nourriture, à l’intérieur des organismes. Ensuite, par le processus de bioamplification*, le mercure s’accumule dans les organismes aux niveaux supérieurs des réseaux trophiques5,6. La bioamplification se produit quand le niveau de contamination est plus élevé dans les prédateurs que dans les proies au sein d’un réseau trophique (voir fig. 2).
Après sa transformation en méthylmercure, notre atome de mercure se retrouve à l’intérieur d’un phytoplancton. Ce dernier est ingéré par un invertébré benthique, une petite larve vivant dans les sédiments, et par des centaines d’autres algues. Par la suite, un jeune omble de l’Arctique ingère des centaines d’invertébrés aquatiques, dont cette petite larve, accumulant encore plus de méthylmercure dans ses muscles et son foie. Plusieurs de ces jeunes poissons se font cannibaliser par un seul grand omble, et ainsi le niveau de contamination augmente au fur et à mesure que l’on s’élève dans le réseau trophique6,7.
Quand un pêcheur inuit mange un omble de l’Arctique contaminé, le mercure qu’il contient entre donc dans son sang, est transporté à travers le corps, puis traverse la barrière hématoencéphalique pour entrer dans son cerveau. C’est ainsi que l’atome de mercure se retrouve, trois ans après son départ de la mine de charbon chinoise, lié à une protéine dans le cerveau d’un pêcheur inuit dans le nord du Canada.
Influence des changements climatiques sur le mercure dans l’Arctique
De toute évidence, l’Arctique subit de très grands changements environnementaux liés aux changements climatiques. Les tendances de réchauffement climatique sont amplifiées à hautes latitudes et les zones tempérées et les écosystèmes arctiques sont sensibles à ce changement8. Au cours des 100 dernières années, l’ensemble de notre planète a subi un réchauffement de la température moyenne annuelle de 0,85 °C, mais en Arctique, la température augmente deux fois plus rapidement qu’ailleurs sur la planète et de vastes régions nordiques se sont réchauffées de l’ordre de 5 °C8,9.
Pourtant, les effets des changements climatiques sur le cycle de mercure sont toujours incertains, puisque les impacts des changements climatiques sur l’environnement sont extrêmement complexes, rapides et difficiles à prédire avec précision4. Ce que nous savons, c’est que la réponse des écosystèmes nordiques aux changements sera probablement très variable géographiquement et que le transport, la transformation et le transfert de mercure dans l’environnement risquent de changer de façon importante. Des recherches plus approfondies sont nécessaires pour comprendre si un réchauffement augmentera ou diminuera la charge en mercure chez les organismes aquatiques et chez les peuples de l’Arctique.
Une préoccupation pour tous
Mieux comprendre le cycle du mercure dans le Nord est primordial afin de réduire, voire éviter les risques que pose cette toxine pour la santé des peuples autochtones de l’Arctique. Avec une alimentation traditionnelle composée de poisson, de baleine et de phoque, ces peuples sont vulnérables à une exposition élevée en mercure. Pourtant, cette nourriture traditionnelle est essentielle à leur vie, faisant partie intégrante de leurs cultures et traditions1. Il importe également que l’Arctique soit la région de la planète où les changements climatiques se font ressentir en premier, une sorte d’exemple des changements à venir8. L’Arctique est donc une région indicatrice, un immense laboratoire en milieu naturel qui nous indique déjà les nombreuses conséquences néfastes d’une contamination environnementale à grande échelle. Une meilleure compréhension des dynamiques du mercure dans l’Arctique nous permettrait de prévenir que les conséquences de cette contamination se retrouvent chez nous, dans les régions plus peuplées du Sud. La santé écosystémique et humaine de l’Arctique est un excellent indicateur de la santé de notre planète dans son ensemble.
Remerciements
Merci à Marc Amyot, directeur du département de sciences biologiques de l’Université de Montréal, pour son aide avec la rédaction de cet article.
GLOSSAIRE
BCP : Les biphényles polychlorés (BCP) sont des composés organochlorés synthétiques utilisés dans une vaste gamme d’activités industrielles, surtout dans les transformateurs et condensateurs électriques et dans la production des plastiques, peintures et pesticides.
Bioaccumulation : Le processus d’accumulation d’une substance (souvent une substance toxique) dans tout ou une partie d’un organisme (mesuré à l’échelle de l’organisme).
Bioamplification : Le processus de rétention d’une substance dans les tissus des organismes, à des teneurs de plus en plus élevées au fur et à mesure que l’on s’élève dans des réseaux trophiques (mesurée à l’échelle des réseaux trophiques).
Changements climatiques : Le réchauffement climatique est un phénomène d’augmentation de la température moyenne des océans et de l’atmosphère observé depuis le début du XXe siècle, mesuré à l’échelle mondiale sur plusieurs décennies, et qui traduit par une augmentation de la quantité de chaleur de la surface terrestre.
DDT : Le dichlorodiphényltrichloroéthane (DDT) est probablement le plus tristement célèbre de tous les insecticides synthétiques. Il a été largement répandu pour le contrôle de la malaria et du typhus et il a aussi été utilisé intensivement dans la culture de coton. Le DDT présente toujours un danger environnemental élevé, car il est hautement toxique et persistant.
Écotoxicologie (adj. écotoxicologique) : Une discipline dans les sciences biologiques située à l’interface entre l’écologie et la toxicologie, et qui étudie les conséquences écologiques de la contamination chimique, biologique ou radioactive.
Semi-volatil : Une substance chimique semi-volatile a tendance à se vaporiser (à s’évaporer) aux températures relativement basses, mais aux températures plus élevées que les substances volatiles. Ces substances chimiques peuvent facilement se trouver sous forme gazeuse dans l’atmosphère.
Réseau trophique : L’ensemble des relations trophiques et des chaînes alimentaires interconnectées qui existent dans un groupe multispécifique d’êtres vivants. Une chaîne alimentaire ou trophique est une série d’espèces vivantes, dans laquelle les organismes cités en premier lieu sont mangés par ceux qui les suivent, qui seront à leur tour mangés par les suivants.
RÉFÉRENCES
1AMAP. Assessment 2011: Mercury in the Arctic. Arctic Monitoring and Assessment Program and Arctic Pollution, Oslo, AMAP, 2011.
2Muir D, Braune B, DeMarch B, Norstrom R, Wagemann R, Lockhart L, et coll. « Spatial and Temporal Trends and Effects of Contaminants in the Canadian Arctic Marine Ecosystem: A Review », Science of the Total Environ, vol. 230, 1999, p. 83-144.
3UNEP. Global Mercury Assessment 2013, Sources, Emissions, Releases and Environmental Transport. UNEP Chemicals Branch, Geneva, Switzerland, 2013.
4 Stern G.A. et coll. (2012). « How Does Climate Change Influence Arctic Mercury? » Science of the Total Environment, vol. 414, p. 22-42.
5Steffen, A., Douglas, T., Amyot, M., Ariya, P., Aspmo, K., & Berg, T. « A Synthesis of Atmospheric Mercury Depletion Event Chemistry Linking Atmosphere , Snow and Water », Environmental Research, no 7, 2007, p. 10837-10931.
6Wiener, J. G., Krabbenhoft, D. P., Heinz, G. H., Drive, A. H., & Scheuhammer, A. M. « Ecotoxicology of Mercury », Wildlife Research, vol. 16, nov. 2002, p. 409- 463.
7 Kidd K. Clayden M. et Jardine T. « Bioaccumulation and Biomagnification of Mercury through Food Webs », dans Environmental Chemistry and Toxicology of Mercury. Guangliang Liu, Yong Cai, et Nelson O’Driscoll, New York, John Wiley & Sons (dir.), c2012, chapitre 14, p. 455-487.
8 Serreze, M. C., et Francis, J. A. « The Arctic Amplification Debate », Climatic Change, vol. 76, 2006, p. 241-264.
9 IPCC. Climate Change 2007: Impacts, Adaptation and Vulnerability. Contributions of Working Group II to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change, M.L. Parry, O.F Canziani, J.P. Palutikof, P.J. van der Linden et C.E. Hanson (dir.), Cambridge, Cambridge University Press, 2007, p. 653-685.