Hormis la chirurgie, le cancer a connu deux grandes révolutions thérapeutiques : la chimiothérapie et les thérapies dites « ciblées ». Malgré les retombées importantes de ces percées, la maladie demeure souvent lourde de conséquences. Une troisième révolution s’annonce : l’immunothérapie du cancer, soit l’utilisation du système immunitaire de l’hôte pour rejeter le cancer ! Cette nouvelle prouesse scientifique saura-t-elle combler toutes les attentes ?
Des tumeurs avaient probablement été observées bien avant, mais le médecin égyptien Imhotep a été le premier à répertorier des cas de cancer, dans ce qui est appelé aujourd’hui le papyrus Edwin Smith, il y a plus de 4 000 ans[1]. D’innombrables études scientifiques ont par la suite ciblé la maladie, sans toutefois en éclairer tous les mécanismes. Pendant plusieurs siècles (et jusqu’à récemment), la chirurgie représentait la seule intervention thérapeutique réellement valable. En effet, depuis longtemps, le corps médical considère que le retrait des tumeurs doit être pratiqué tôt dans le développement de la maladie, sans quoi le cancer risque de se propager dans l’organisme. Ce n’est par contre qu’au cours des cent dernières années que des traitements de rechange sont apparus et, depuis, ils ne cessent de se renouveler. L’immunothérapie, récemment ajoutée à l’arsenal médical, réussira peut-être alors à mettre fin à cette lutte incessante.
Des cellules qui se multiplient… trop
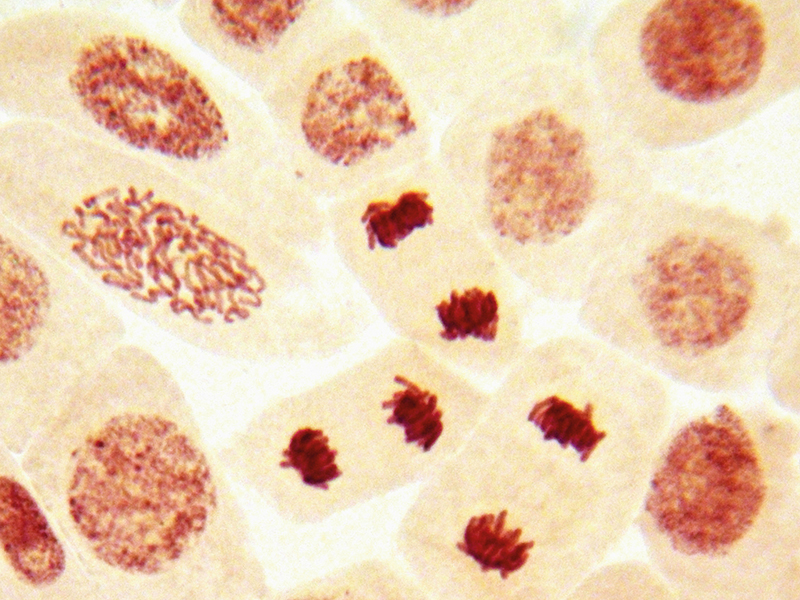
Le cancer est caractérisé par une croissance incontrôlée des cellules, qui sont les chefs d’orchestre de tous les processus physiologiques des êtres vivants. Elles occupent des fonctions diverses, et certaines d’entre elles sont aptes à proliférer. Fort heureusement, les cellules saines ne peuvent pas se répliquer indéfiniment, puisqu’elles sont soumises à différents mécanismes de régulation. Ces cellules peuvent ainsi se multiplier au besoin, lorsque la croissance ou la régénération normales de l’organisme le requièrent.
Les cellules cancéreuses, quant à elles, sont souvent « sourdes » et « immortelles ». Autrement dit, elles font abstraction de leur environnement et des mécanismes de contrôle, et se reproduisent continuellement, ce qui est problématique. Cette autonomie proliférative et incontrôlée des cellules cancéreuses ainsi que leur instabilité génomique font progresser les cancers[2].
Le génome est la boîte noire de l’information génétique (ADN) qui fait fonctionner une cellule. Il est très sensible aux mutations génétiques, qui surviennent entre autres lors de la réplication cellulaire*. Selon la nature de ces mutations, les cellules sont susceptibles d’acquérir des caractéristiques favorisant l’apparition ou la progression du cancer. En somme, les cellules cancéreuses ne sont que des « versions altérées de nos cellules normales », comme l’a souligné Harold E. Varmus lors d’un discours qu’il a prononcé quand il a reçu le prix Nobel de la médecine en 1989.
Un fait est généralement accepté : la naissance d’une cellule cancéreuse ne constitue pas un événement rare. Notre organisme est même doté d’un système de défense pour s’en prémunir[3]. En effet, le système immunitaire perçoit les cellules cancéreuses comme un danger et les élimine pour inhiber rapidement l’évolution du cancer. Malheureusement, les cellules cancéreuses parviennent bien souvent à déjouer ces défenses naturelles.
La prolifération incontrôlée des cellules cancéreuses
Puisque les cellules cancéreuses sont disposées à proliférer continuellement, pourquoi ne pas simplement les empêcher de se multiplier? C’est le pari qu’a pris Sydney Farber, souvent considéré comme le père de la chimiothérapie moderne, au début du 20e siècle[4]. La chimiothérapie, première révolution parmi les traitements anticancéreux, vise en ce sens à induire des dommages irréversibles à l’ADN, afin de contraindre les cellules cancéreuses à mourir. Cependant, son large spectre d’activité, qui lui confère un avantage considérable, est aussi responsable d’un lourd inconvénient.
En effet, puisque la chimiothérapie agit sur l’aspect prolifératif des cellules cancéreuses, elle peut être employée contre tous types de néoplasmes malins*. Par contre, les cellules cancéreuses n’étant pas les seules à proliférer dans l’organisme, ce type de traitement les distingue difficilement des cellules saines. Il affecte donc aussi ces dernières et cause plusieurs effets indésirables, comme la perte des cheveux et les vomissements. Utiliser efficacement la chimiothérapie, c’est tenter de doser un poison à des fins thérapeutiques.
Les exclusivités moléculaires comme cibles des traitements
En entravant la prolifération, la chimiothérapie ne distingue donc pas totalement les cellules saines des cellules cancéreuses. Les traitements peuvent-ils alors viser d’autres caractéristiques plus exclusives aux cellules cancéreuses ? Les thérapies dites « ciblées », qui constituent la deuxième révolution thérapeutique anticancéreuse, s’attaquent tout particulièrement à ce problème. Elles n’ont été intégrées à l’arsenal thérapeutique que très récemment, soit vers la fin des années quatre-vingt-dix.
Le cancer consiste en fait en une grande famille de maladies dont la nomenclature s’étend bien au-delà de la localisation de la tumeur dans l’organisme. Ainsi, des sous-types de cancers du sein sont classés selon des critères moléculaires : normal, de type basal, HER2 positif, luminal A et luminal B[5]. La thérapie « ciblée » repose alors sur le principe de la détermination des processus influençant la progression de ces différents cancers. Par exemple, les patientes atteintes du cancer du sein HER2 positif sont susceptibles de répondre favorablement à un anticorps nommé « trastuzumab » (commercialisé sous le nom d’« Herceptin »), qui cible et neutralise spécifiquement le récepteur HER2 sur les cellules cancéreuses du sein. Lorsque la protéine HER2 est surexprimée*, les cellules cancéreuses deviennent plus susceptibles de proliférer abondamment et de permettre le développement d’un cancer, d’où l’intérêt de neutraliser spécifiquement HER2.
Le principe des thérapies « ciblées » requiert l’identification des molécules favorisant la croissance de chacun des sous-types de cancer. À ce jour, la Food and Drug Administration (FDA), l’organisme américain qui réglemente notamment les produits pharmaceutiques, a approuvé plus d’une cinquantaine de médicaments du type « thérapie ciblée » visant une vingtaine de cancers différents[6].
Mais au-delà de cette sous-classification basée sur des critères moléculaires, il subsiste une autre source de variabilité entre les cancers : l’interindividualité. Chaque être humain est différent et possède donc un ADN particulier. Ainsi, chaque cancer est singulier, et l’efficacité variable des traitements entre patients en est le reflet. C’est d’ailleurs pourquoi certaines patientes répondront positivement au trastuzumab alors que d’autres non. Autrement dit, ce n’est pas parce que des cellules cancéreuses présentent abondamment le récepteur HER2 que le cancer est nécessairement « conduit » par celui-ci. Le neutraliser sur les cellules cancéreuses du sein HER2 positives ne se solde donc pas systématiquement par un succès thérapeutique.
Le système immunitaire et le cancer : le chat et la souris
Le système immunitaire reconnaît et attaque les cellules cancéreuses émergentes. Aussi, plutôt que de se concentrer sur l’identification des molécules responsables des cancers, l’immunothérapie repose sur le principe d’éducation du système immunitaire de l’hôte.
De multiples preuves confirment l’importance du système immunitaire dans la réponse de l’organisme en la présence du cancer. En effet, certaines personnes présentent un risque bien plus élevé que d’autres de développer un cancer, comme en témoigne l’augmentation du nombre de cas de sarcome de Kaposi* dans la population atteinte du sida[7]. C’est que les cancers sont plus susceptibles de frapper lorsque le système immunitaire est vulnérable.
Pour mieux comprendre les stratégies qui permettent d’utiliser le système immunitaire de l’hôte pour lutter contre la maladie, il importe de comprendre comment les cellules cancéreuses parviennent à échapper aux lymphocytes, ces cellules sanguines qui constituent les défenses naturelles du corps. Les lymphocytes ont pour fonction de repérer les corps étrangers et d’en débarrasser l’organisme. Puisque les cellules cancéreuses résultent en fait d’une transformation de cellules saines et ne proviennent donc pas de l’extérieur de l’organisme, comment faire en sorte que le système immunitaire détecte leur présence ?
Les cellules de l’organisme présentent à leur surface des antigènes* définissant leur identité. Ces « cartes d’identité » leur permettent d’être tolérées par le système immunitaire. Ainsi, un corps étranger présentant une « carte d’identité » différente sera rapidement identifié et neutralisé par les défenses immunes. Puisqu’elles contiennent des informations génétiques altérées, les cellules cancéreuses sont susceptibles de générer des protéines mutantes*. Ces nouvelles protéines cancéreuses, appelées « antigènes tumoraux », modifieront la « carte d’identité » de ces cellules et les rendront vulnérables face aux mécanismes de défense de l’organisme.
Le système immunitaire et le cancer : quand le chat n’est pas là, les souris dansent
Alors que l’organisme possède des mécanismes pour réagir aux cellules cancéreuses et amorcer une réponse immunitaire antitumorale, ces dernières utilisent divers moyens pour échapper à sa surveillance. Entre autres, elles peuvent présenter à leur surface des molécules qui permettent l’inactivation des lymphocytes antitumoraux, et parviennent alors à atténuer la réponse immunitaire contre le cancer. Autrement dit, les lymphocytes continuent à reconnaître les cellules tumorales, mais tolèrent leur présence !
Certaines études semblent, par ailleurs, démontrer que de bloquer ces mécanismes d’inactivation pourrait être efficace afin de rétablir l’activité du système immunitaire contre le cancer[8]. L’approbation par la FDA en 2011 de l’ipilimumab (commercialisé sous le nom de « Yervoy »), un anticorps dirigé contre le récepteur CTLA-4 dans le traitement du mélanome métastatique*, représente en ce sens une première victoire de l’immunothérapie du cancer et ouvre la porte à l’arrivée de nouveaux traitements du même type. Plusieurs essais cliniques sont également en cours pour vérifier si l’ipilimumab pourrait être utilisé contre d’autres types de cancers, dont celui de la prostate et certains cancers du poumon[9]. De nombreuses autres molécules prometteuses sont aussi en développement et devraient faire leur apparition très prochainement en Amérique. Il n’est d’ailleurs pas anodin que la prestigieuse revue Science, de l’American Association for the Advancement of Science, ait reconnu l’immunothérapie du cancer comme la plus grande avancée médicale de l’année 2013 !
L’immunothérapie du cancer : oui, mais…
Malgré tout, l’avènement de l’immunothérapie ne signifie pas nécessairement le rejet des traitements traditionnels anticancéreux. Bien que grandement prometteuse, l’immunothérapie n’est pas vouée à un succès absolu et n’est pas dépourvue d’effets indésirables. Beaucoup reste encore à découvrir concernant la cure contre cet ennemi redoutable qu’est le cancer. Pour maximiser les chances de guérison, minimiser les risques de résistance thérapeutique et amoindrir les effets indésirables des traitements, combiner plusieurs stratégies anticancéreuses demeure et demeurera probablement l’option la plus profitable.
Lexique
Antigène : molécule susceptible d’induire une réponse immunitaire.
Mélanome métastatique : type de cancer de la peau qui se dissémine dans l’organisme.
Néoplasme malin : tumeur cancéreuse agressive et susceptible de se généraliser, représentant une menace à la survie d’un organisme.
Protéine mutante : protéine dont la composition diffère de la protéine habituelle.
Réplication cellulaire : processus de division cellulaire par lequel le matériel génétique se reproduit sous la même forme dans le but de générer une nouvelle cellule.
Surexpression : expression anormalement élevée, souvent pathologique, d’une protéine à la surface d’une cellule.
Sarcome de Kaposi : type de cancer de la peau extrêmement rare dans la population immunocompétente.
[1] MUKHERJEE, Siddhartha. The Emperor of All Maladies: A Biography of Cancer, New York, Scribner, 2010.
[2] HANAHAN, Douglas et Robert A. WEINBERG. « Hallmarks of cancer: The next generation », Cell Press, vol. 144, no 5, mars 2011, p. 646-674.
[3] DUNN, Gavin P., Allen T. BRUCE, Hiroaki IKEDA, Lloyd J. OLD et Robert D. SCHREIBER. « Cancer immunoediting: from immunosurveillance to tumor escape », Nature Immunology, vol. 3, no 11, novembre 2002, p. 991-998.
[4] MUKHERJEE, op. cit.
[5] National Cancer Institute. « Breast cancer », http://www.cancer.gov/cancertopics/types/, page consultée le 9 juillet 2014.
[6] National Cancer Institute, « Targeted Cancer Therapies », http://www.cancer.gov/, page consultée le 9 juillet 2014.
[7] OLIVEIRA COBUCCI, Ricardo N., Humberto SACONATO, Paulo H. LIMA, Hugo M. RODRIGUES, Tardelli L. PRUDENCIO, José E. JUNIOR et collab. « Comparative incidence of cancer in HIV-AIDS patients and transplant recipients », Cancer Epidemiology, vol. 36, no 2, avril 2012, p. e69-e73.
[8] SAKUISHI, Kaori, Lionel APETOH, Jenny M. SULLIVAN, Bruce R. BLAZAR, Vijay K. KUCHROO et Ana C. ANDERSON. « Targeting Tim-3 and PD-1 pathways to reverse T cell exhaustion and restore anti-tumor immunity », Journal of Experimental Medicine, vol. 207, no 10, septembre 2010, p. 2187-2194.
[9] « ClinicalTrials.gov » [base de données sur les essais cliniques aux États-Unis], http://www.clinicaltrials.gov/ct2, page consultée le 9 juillet 2014.