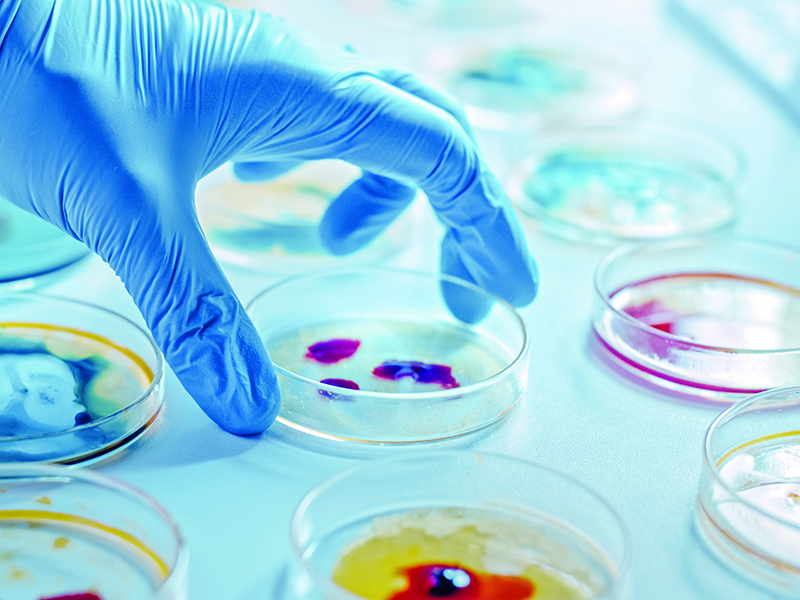
Selon l’Organisation mondiale de la santé, plus d’un milliard de personnes vivent dans une zone à risque pour la leishmaniose, une maladie infectieuse qui affecte principalement le foie et la rate et qui entraîne une fièvre, des faiblesses et, éventuellement, la mort. La capacité du parasite qui cause cette affection à devenir rapidement résistant aux traitements constitue le plus grand obstacle à son éradication. L’adaptation de ce microorganisme peut d’ailleurs rendre inefficace un traitement chez un patient. Le repositionnement de médicament, soit le fait de réutiliser un médicament existant pour traiter d’autres maladies que celle déjà ciblée par celui-ci, s’annonce une approche prometteuse. Dans le laboratoire de parasitologie de la Faculté de médecine vétérinaire de l’Université de Montréal, un traitement d’abord utilisé contre le cancer est au banc d’essai contre la leishmaniose.
L’aspirine est l’exemple le plus célèbre du repositionnement de médicament. Elle a été synthétisée en 1897 par le chimiste allemand Felix Hoffman pour traiter les douleurs et la fièvre. Aujourd’hui, grâce à la découverte de ses propriétés anticoagulantes, l’aspirine est aussi utilisée pour traiter de multiples maladies cardiovasculaires[1]. Afin de répondre au manque d’options thérapeutiques contre la leishmaniose, les scientifiques veulent tirer parti du repositionnement de médicament, une stratégie qui a déjà fait ses preuves. C’est donc dans cette optique que des chercheurs, notamment ceux du laboratoire du professeur Christopher Fernandez Prada à la Faculté de médecine vétérinaire de l’Université de Montréal, étudient le topotécan, utilisé à l’origine en tant qu’antitumoral*, comme solution en cas d’échec au traitement chez un patient atteint de la leishmaniose. Cependant, pour éviter que le parasite devienne résistant à ce nouveau traitement potentiel, des études en laboratoire doivent d’abord être menées. De cette façon, le personnel médical pourra en faire une utilisation clinique judicieuse qui permettra de conserver le plus longtemps possible l’efficacité du topotécan comme médicament contre la leishmaniose.
La conception de nouveaux médicaments
Trop lent pour répondre aux besoins actuels, le processus conventionnel de production des médicaments se divise en deux temps : la découverte de nouvelles molécules, puis le développement de celles-ci. En premier lieu, les scientifiques définissent les cibles. Celles-ci représentent les causes de la maladie observée ; elles peuvent être un gène en particulier, une protéine produite par le corps ou un microorganisme, tel le parasite dans le cas de la leishmaniose. Une fois ce travail terminé, l’affinité entre les molécules, au nombre de près de 10 000 en moyenne au début du processus, et la cible est confirmée, le plus souvent par des modélisations informatiques. Cette sélection initiale dure plus de quatre ans. Après cette étape seulement, le développement dans les laboratoires peut débuter. Des modifications biochimiques préliminaires pourront être apportées au besoin pour modifier certains paramètres tels que l’absorption ainsi que la distribution de la molécule dans le corps et son élimination[2].
Si un composé est prometteur, il passe ensuite en phase préclinique. À ce stade, seulement une vingtaine sur les 10 000 du départ sont encore présents dans la course. C’est à ce moment que les scientifiques déterminent l’effet du composé sur la cible, le parasite dans le cas de la leishmaniose. Au début, les tests s’effectuent in vitro*, puis si les résultats sont concluants, la phase préclinique se poursuit sur les animaux de laboratoire après l’approbation d’un plan d’essai par différents groupes tels que le Comité d’éthique de la recherche de Santé Canada et de l’Agence de la santé publique du Canada. Enfin, les composés qui réussissent la phase préclinique, soit seulement la moitié d’entre eux, passeront à la troisième étape, c’est-à-dire la phase clinique.
En moyenne, au moment où se termine la phase clinique, 11 ans se seront écoulés depuis le début du processus, et après avoir soumis toute l’information nécessaire au gouvernement, les laboratoires devront attendre plus d’un an avant d’obtenir le permis de mise en marché du produit. Au Canada, l’organisme qui approuve les nouveaux médicaments est Santé Canada. Cette instance a le dernier mot et peut imposer certaines restrictions d’usage au nouveau médicament. Elle peut même refuser l’homologation* de ce dernier. Une fois toutes ces étapes franchies, pour que la population puisse bénéficier de ce nouveau médicament, le laboratoire devra le produire et le distribuer en quantité suffisante pour répondre à la demande[3] (voir figure 1). Cette dernière étape impose des contraintes de temps supplémentaires, puisque certaines maladies telles que la leishmaniose sévissent dans des contextes socioéconomiques précaires. En effet, l’Organisation mondiale de la santé considère la leishmaniose comme une maladie tropicale négligée. Ce type de maladie touche principalement les populations les plus démunies du globe et, puisque celles-ci ont en général un pouvoir politique diminué, le grand public se préoccupe peu de ces maladies.
Ligne du temps et des stades de développement pour un produit pharmaceutique (moyenne industrielle)
Source : GlaxoSmithKline. (2018). How we discover new medicines. https://www.gsk.com/en-gb/research-and-development/development/how-we-develop-new-medicines/
Le repositionnement de médicament
Présentement, le traitement le plus utilisé contre la leishmaniose est l’antimoine*, un élément chimique qui ressemble à l’arsenic. Cependant, la résistance grandissante du parasite à ce médicament engendre des échecs au traitement. À titre d’exemple, au Bihar, une région de l’Inde fortement touchée par la leishmaniose, plus de 60 % des patients ne répondent plus au traitement[4]. Devant l’urgence de la situation, différentes stratégies ont été mises en place au cours des dernières années. Afin de contrôler cette maladie, les chercheurs tentent de tirer avantage du repositionnement de médicament, mieux connu sous son appellation anglaise drug repurposing. Cette façon de faire est à la hausse depuis un certain temps, totalisant 30 % des nouveaux traitements approuvés par la U.S. Food and Drug Administration[5]. Plusieurs avantages rendent le repositionnement de médicament plus profitable que le développement complet d’une nouvelle molécule. Il permet de diminuer le délai, puisque le médicament a précédemment subi les essais précliniques chez les animaux, la sécurité du produit a auparavant été validée et, parfois, le développement de la formulation aura même déjà été réalisé[6].
En moyenne, le repositionnement de médicament prendrait 6,5 ans, soit environ la moitié du temps habituellement requis pour développer un nouveau médicament. Pour les mêmes raisons, cette méthode permet souvent de réduire de façon importante l’investissement financier total. Le coût de développement d’un nouveau médicament se situerait entre 2 et 3 milliards de dollars américains, tandis que la réutilisation d’un médicament pour une nouvelle homologation en coûterait environ 300 millions[7]. En d’autres mots, cette méthode de développement de nouveaux médicaments offre une prise de risque faible pour un rendement potentiel élevé.
Une alternative médicamenteuse
Aujourd’hui, l’antimoine pentavalent constitue le traitement de première ligne pour traiter la leishmaniose, tant en médecine vétérinaire qu’en médecine humaine. En raison de ses multiples effets secondaires, trop souvent des doses sous-thérapeutiques sont administrées au patient et fréquemment, des abandons en cours de traitement surviennent. Ces tendances, jumelées à une qualité inconstante du principe actif du médicament, contribuent à l’émergence de la résistance du parasite envers l’antimoine pentavalent[8]. Selon la théorie de l’évolution des espèces élaborée par Charles Darwin, au sein d’une population donnée, des variations naturelles existent entre les individus d’une même espèce, ce qui leur permet de répondre plus ou moins adéquatement à leur environnement. Les mieux adaptés survivront et se reproduiront, transmettant ainsi les caractéristiques gagnantes à leurs descendants[9]. C’est aussi de cette manière que se développe la résistance aux antimicrobiens : face à une pression médicamenteuse, certains parasites de la population pourront survivre grâce à un gène de résistance qui sera alors transmis aux autres parasites descendants. Afin de ralentir ce phénomène, qui constitue le problème principal à l’origine de la course pour un nouveau médicament contre la leishmaniose, les chercheurs tentent de proposer une alternative médicamenteuse qui n’aurait pas le même mécanisme d’action sur le parasite que les traitements actuellement utilisés. Ainsi, les risques de résistance croisée* seront diminués.
Dans le cas de la leishmaniose, plusieurs médicaments de différentes classes ont été étudiés attentivement dans les dernières années. La classe de médicaments qui semble la plus prometteuse à ce jour est celle des antitumoraux, qui agissent sur les cellules qui se répliquent à une très grande vitesse, comme les cellules cancéreuses. En effet, un grand nombre de médicaments de cette classe ont démontré des activités in vitro contre le parasite[10], justement parce qu’ils peuvent cibler certains microorganismes, qui se multiplient eux aussi à une très grande vitesse. Le topotécan déjà homologué et utilisé contre plusieurs types de cancers en Amérique du Nord constitue une option de choix. Son activité antileishmaniale a déjà été prouvée en laboratoire : il cible les topoisomérases*, des enzymes essentielles au fonctionnement cellulaire du parasite[11]. La stratégie du repositionnement de médicament permettrait d’obtenir rapidement un nouveau traitement efficace abordable en cas d’échec avec l’antimoine pentavalent chez un patient. Afin d’éviter de répéter les mêmes erreurs qui ont mené à une émergence rapide de la résistance du parasite à l’antimoine pentavalent, plusieurs groupes de chercheurs s’affairent à étudier les modifications génomiques chez Leishmania lorsqu’il est soumis à la pression médicamenteuse du topotécan. Si la résistance est bien anticipée en laboratoire, les conséquences sur le terrain pourront être amoindries et mieux contrôlées.
Une option prometteuse
C’est d’ailleurs grâce au repositionnement de médicament qu’il y a plus de quatre-vingts ans, l’antimoine a été le premier médicament approuvé pour traiter la leishmaniose[12]. Encore aujourd’hui, devant l’émergence de la résistance, les chercheurs s’appuient à nouveau sur cette stratégie pour trouver de nouvelles options thérapeutiques abordables, et ce, en peu de temps. La communauté scientifique internationale s’est récemment intéressée aux antitumoraux comme le topotécan pour traiter cette maladie et les résultats sont prometteurs. Plusieurs autres conditions médicales pourraient bénéficier du repositionnement de médicament dans les années futures. Par exemple, depuis le début de la pandémie de COVID-19 qui paralyse présentement le monde entier, l’équipe du docteur Jean-Claude Tardif de l’Institut de cardiologie de Montréal s’intéresse à la colchicine comme traitement afin de prévenir les complications sévères de la COVID-19. La colchicine est, à l’origine, un anti-inflammatoire utilisé depuis de nombreuses années pour traiter des maladies inflammatoires telles que la goutte[13]. Dans l’attente d’un vaccin efficace contre la COVID-19, un médicament rapidement accessible contre cette maladie faciliterait la gestion de cette crise sanitaire.
Lexique :
*Antitumoral : médicament administré pour combattre les tumeurs.
*In vitro : qui a lieu en milieu artificiel.
*Antimoine : élément chimique de la classe des métalloïdes qui porte le numéro atomique 51.
*Homologation : processus par lequel une instance gouvernementale certifie qu’un médicament est conforme et peut être utilisé en toute sécurité pour une condition médicale donnée.
*Résistance croisée : aptitude d’un microorganisme à résister à un médicament auquel il n’a jamais été exposé en raison de son exposition antérieure à un autre médicament similaire.
*Topoisomérase : enzyme qui permet de relâcher le matériel génétique hautement condensé dans le noyau de la cellule.
Références
[1] Montinari, M. R., Minelli, S. et De Caterina, R. (2018). The first 3500 years of aspirin history from its roots – A concise summary. Vascular Pharmacology, 113, 1-8. https://doi.org/10.1016/j.vph.2018.10.008
[2] Duelen, R., Corvelyn, M., Tortorella, I., Leonardi, L., Chai, Y. C. et Sampaolesi, M. (2019). Medicinal biotechnology for disease modeling, clinical therapy, and drug discovery and development. Dans F. Matei et D. Zirra (dir.), Introduction to biotech entrepreneurship: From idea to business (p. 89-128). https://doi.org/10.1007/978-3-030-22141-6_5
[3] GlaxoSmithKline. (2018). How we discover new medicines. https://www.gsk.com/en-gb/research-and-development/development/how-we-develop-new-medicines/
[4] Stauch, A., Duerr, H.-P., Dujardin, J.-C., Vanaerschot, M., Sundar, S. et Eichner, M. (2012). Treatment of visceral leishmaniasis: Model-based analyses on the spread of antimony-resistant L. donovani in Bihar, India. PLoS Neglected Tropical Diseases, 6(12), e1973. https://doi.org/10.1371/journal.pntd.0001973
[5] Jin, G. et Wong, S. T. C. (2014). Toward better drug repositioning: Prioritizing and integrating existing methods into efficient pipelines. Drug Discovery Today, 19(5), 637-644. https://doi.org/10.1016/j.drudis.2013.11.005
[6] Pushpakom, S., Iorio, F., Eyers, P. A., Escott, K., Hopper, S., Wells, A., Doig, A., Guilliams, T., Latimer, J., McNamee, C., Norris, A., Sanseau, P., Cavalla, D. et Pirmohamed, M. (2019). Drug repurposing: Progress, challenges and recommendations. Nature, 18(1), 41-58. https://doi.org/10.1038/nrd.2018.168
[7] Nosengo, N. (2016). Can you teach old drugs new tricks? Nature, 534(7607), 314-316.
[8] Barrett, M. P. et Croft, S. L. (2012). Management of trypanosomiasis and leishmaniasis. British Medical Bulletin, 104(1), 175-196. https://doi.org/10.1093/bmb/lds031
[9] L’Origine des espèces. (2020, 8 juin). Dans Wikipédia.https://fr.wikipedia.org/wiki/L%27Origine_des_esp%C3%A8ces
[10] Andrade-Neto, V. V., Ferreira Cunha-Junior, E., dos Santos Faioes, V., Pereira Martins, T., Lopes Silva, R., Laura Leon, L. et Caio Torres-Santos, E. (2018). Leishmaniasis treatment: Update of possibilities for drug repurposing. Frontiers in Bioscience, 23, 967-996. https://doi.org/10.2741/4629
[11] Prada, C. F., Álvarez-Velilla, R., Balaña-Fouce, R., Prieto, C., Calvo-Álvarez, E., Escudero-Martínez, J. M., Requena, J. M., Ordóñez, C., Desideri, A., Pérez-Pertejo, Y. et Reguera, R. M. (2013). Gimatecan and other camptothecin derivatives poison Leishmania DNA-topoisomerase IB leading to a strong leishmanicidal effect. Biochemical Pharmacology, 85(10), 1433-1440. https://doi.org/10.1016/j.bcp.2013.02.024
[12] Frézard, F., Monte-Neto, R. et Reis, P. G. (2014). Antimony transport mechanisms in resistant leishmania parasites. Biophysical Reviews, 6(1), 119-132. https://doi.org/10.1007/s12551-013-0134-y
[13] Meloche-Holubowski, M. (2020, 22 mars). Début d’une étude clinique pour tester un médicament contre les effets de la COVID-19. ICI Radio-Canada. https://ici.radio-canada.ca/nouvelle/1681600/traitement-coronavirus-covid19-tardif-montreal-canada-quebec-colcorona